Auteur:
Bobbie Johnson
Date De Création:
10 Avril 2021
Date De Mise À Jour:
1 Juillet 2024
Contenu
- Pas
- Partie 1 sur 2: Préparer l'équipement
- Partie 2 sur 2: Mener une expérience
- Conseils
- Avertissements
- De quoi avez-vous besoin
Processus de fractionnement de l'eau (H2O) en ses constituants (hydrogène et oxygène) à l'aide d'électricité est appelée électrolyse. Les gaz obtenus à la suite de l'électrolyse peuvent être utilisés seuls - par exemple, l'hydrogène est l'une des sources d'énergie les plus propres. Bien que le nom de ce processus puisse sembler un peu intelligent, il est en fait plus facile qu'il n'y paraît si vous avez le bon équipement, les connaissances et un peu d'expérience.
Pas
Partie 1 sur 2: Préparer l'équipement
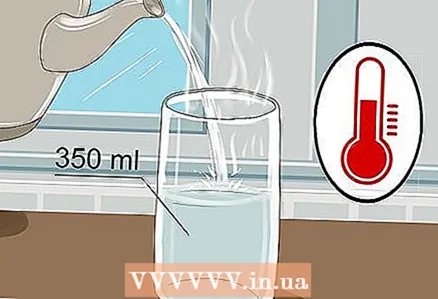 1 Prenez un verre de 350 ml et versez-y de l'eau tiède. Il n'est pas nécessaire de remplir le verre à ras bord, juste un peu d'eau suffit. L'eau froide fera l'affaire, bien que l'eau chaude conduise mieux l'électricité.
1 Prenez un verre de 350 ml et versez-y de l'eau tiède. Il n'est pas nécessaire de remplir le verre à ras bord, juste un peu d'eau suffit. L'eau froide fera l'affaire, bien que l'eau chaude conduise mieux l'électricité. - L'eau du robinet et l'eau en bouteille feront l'affaire.
- L'eau chaude a une viscosité plus faible, ce qui facilite le déplacement des ions.
 2 Dissoudre 1 cuillère à soupe (20 grammes) de sel de table dans de l'eau. Versez le sel dans un verre et remuez l'eau pour la dissoudre. Cela créera une solution saline.
2 Dissoudre 1 cuillère à soupe (20 grammes) de sel de table dans de l'eau. Versez le sel dans un verre et remuez l'eau pour la dissoudre. Cela créera une solution saline. - Le chlorure de sodium (c'est-à-dire le sel de table) est un électrolyte qui augmente la conductivité électrique de l'eau. En soi, l'eau ne conduit pas bien l'électricité.
- Après avoir augmenté la conductivité électrique de l'eau, le courant créé par la batterie traversera plus facilement la solution et décomposera plus efficacement les molécules en hydrogène et oxygène.
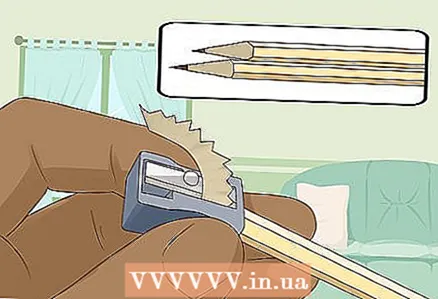 3 Aiguisez deux crayons durs-mous aux deux extrémités pour exposer la mine. N'oubliez pas de retirer la gomme de vos crayons. Une tige de graphite doit dépasser aux deux extrémités.
3 Aiguisez deux crayons durs-mous aux deux extrémités pour exposer la mine. N'oubliez pas de retirer la gomme de vos crayons. Une tige de graphite doit dépasser aux deux extrémités. - Les tiges de graphite serviront d'électrodes isolées auxquelles vous connecterez la batterie.
- Le graphite est bien adapté à cette expérience car il ne se dissout pas et ne se corrode pas dans l'eau.
 4 Découpez une feuille de carton assez grande pour la poser sur le verre. Utilisez un morceau de carton assez épais qui ne s'affaisse pas après avoir percé deux trous. Découpez un morceau carré dans une boîte à chaussures ou similaire.
4 Découpez une feuille de carton assez grande pour la poser sur le verre. Utilisez un morceau de carton assez épais qui ne s'affaisse pas après avoir percé deux trous. Découpez un morceau carré dans une boîte à chaussures ou similaire. - Le carton sert à maintenir les crayons dans l'eau afin qu'ils ne touchent pas les côtés et le fond du verre.
- Le carton n'est pas conducteur, vous pouvez donc le poser en toute sécurité sur un verre.
 5 Utilisez des crayons pour percer deux trous dans le carton. Percez le carton avec des crayons - dans ce cas, ils seront bien serrés et ne glisseront pas. Assurez-vous que le graphite ne touche pas les côtés ou le fond du verre, sinon il interférera avec l'expérience.
5 Utilisez des crayons pour percer deux trous dans le carton. Percez le carton avec des crayons - dans ce cas, ils seront bien serrés et ne glisseront pas. Assurez-vous que le graphite ne touche pas les côtés ou le fond du verre, sinon il interférera avec l'expérience.
Partie 2 sur 2: Mener une expérience
 1 Connectez un fil avec des pinces crocodiles à chaque borne de batterie. La batterie servira de source de courant électrique, et à travers les fils avec des pinces et des tiges de graphite, le courant atteindra l'eau.Connectez un fil avec une pince au positif et l'autre à la borne négative de la batterie.
1 Connectez un fil avec des pinces crocodiles à chaque borne de batterie. La batterie servira de source de courant électrique, et à travers les fils avec des pinces et des tiges de graphite, le courant atteindra l'eau.Connectez un fil avec une pince au positif et l'autre à la borne négative de la batterie. - Utilisez une batterie de 6 volts. Si vous n'en avez pas, vous pouvez utiliser une pile 9 volts à la place.
- Une batterie appropriée peut être obtenue dans un magasin de fournitures électriques ou un supermarché.
 2 Connectez les autres extrémités des fils aux crayons. Fixez fermement les pinces métalliques aux tiges de graphite. Vous devrez peut-être retirer un peu plus de bois des crayons pour empêcher les clips de glisser des tiges de graphite.
2 Connectez les autres extrémités des fils aux crayons. Fixez fermement les pinces métalliques aux tiges de graphite. Vous devrez peut-être retirer un peu plus de bois des crayons pour empêcher les clips de glisser des tiges de graphite. - Ainsi, vous fermerez le circuit et le courant de la batterie traversera l'eau.
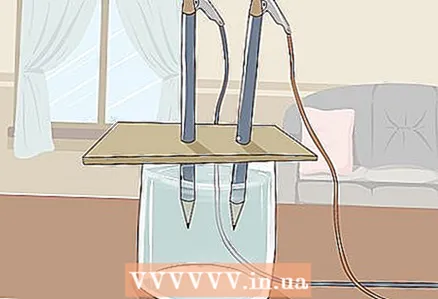 3 Placez le carton sur le verre de manière à ce que les extrémités libres des crayons soient immergées dans l'eau. La feuille de carton doit être suffisamment grande pour reposer sur le verre. Veillez à ne pas perturber le placement correct des crayons.
3 Placez le carton sur le verre de manière à ce que les extrémités libres des crayons soient immergées dans l'eau. La feuille de carton doit être suffisamment grande pour reposer sur le verre. Veillez à ne pas perturber le placement correct des crayons. - Pour que l'expérience soit réussie, le graphite ne doit pas toucher les parois et le fond du verre. Vérifiez à nouveau et ajustez les crayons si nécessaire.
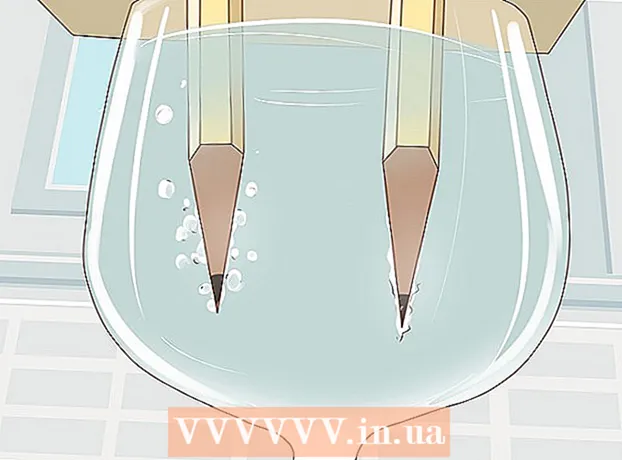
 4 Regardez l'eau se diviser en hydrogène et oxygène. Des bulles de gaz commenceront à s'élever des tiges de graphite immergées dans l'eau. Ce sont l'hydrogène et l'oxygène. De l'hydrogène sera libéré au pôle négatif et de l'oxygène au pôle positif.
4 Regardez l'eau se diviser en hydrogène et oxygène. Des bulles de gaz commenceront à s'élever des tiges de graphite immergées dans l'eau. Ce sont l'hydrogène et l'oxygène. De l'hydrogène sera libéré au pôle négatif et de l'oxygène au pôle positif. - Dès que vous connectez les fils à la batterie et aux tiges de graphite, un courant électrique circulera dans l'eau.
- Plus de bulles de gaz se formeront sur le crayon qui est connecté au pôle négatif, puisque chaque molécule d'eau est composée de deux atomes d'hydrogène et d'un atome d'oxygène.
Conseils
- Si vous n'avez pas de crayons avec des tiges en graphite, vous pouvez utiliser deux petits fils à la place. Enroulez simplement une extrémité de chaque fil autour du pôle correspondant de la batterie et plongez l'autre dans l'eau. Le résultat sera le même qu'avec des crayons.
- Essayez d'utiliser une autre batterie. La quantité de courant circulant dépend de la tension de la batterie, qui, à son tour, affecte le taux de division des molécules d'eau.
Avertissements
- Si vous ajoutez un électrolyte, tel que du sel, à l'eau, gardez à l'esprit que l'expérience générera une petite quantité d'un sous-produit tel que le chlore. Il est sans danger en si petites quantités, mais vous pouvez sentir une légère odeur de chlore.
- Réalisez cette expérience sous la surveillance d'un adulte. Il est associé à l'électricité et aux gaz et peut donc être dangereux, bien que peu probable.
De quoi avez-vous besoin
- Deux crayons durs-doux
- Une batterie 6 ou 9 volts
- Verre d'un volume de 350 millilitres
- 2 fils avec pinces crocodiles
- Taille-crayon pour crayon
- sel